UDIとは?|医療機器向けバーコード?

この記事の目次
医療機器向けの国際ルールUDI対応表示
UDIとは?|医療機器向けの国際ルール
UDI(Unique Device Identification)とは、医療機器の個体管理・個体識別のための国際的な法規則です。*米FDAにより、2013年9月にUDIが公布されて以降、アメリカ・EU諸国からアジア圏まで国際的に採用が始まりました。機器の個体管理・識別を通して医療現場の安全向上や医療機関が最適な治療を提供すること、また流通の効率化が目的とされています。

*FDA(FOOD & DRUG ADMINISTRATION)=米国食品医薬品局 アメリカ国内の食品や医薬品などの法令を定める機関
欧米諸国のUDI規制ではGS1コードを使用して製品の有効期限やロット番号を表示するほか、*データベースへの登録が義務化されています。
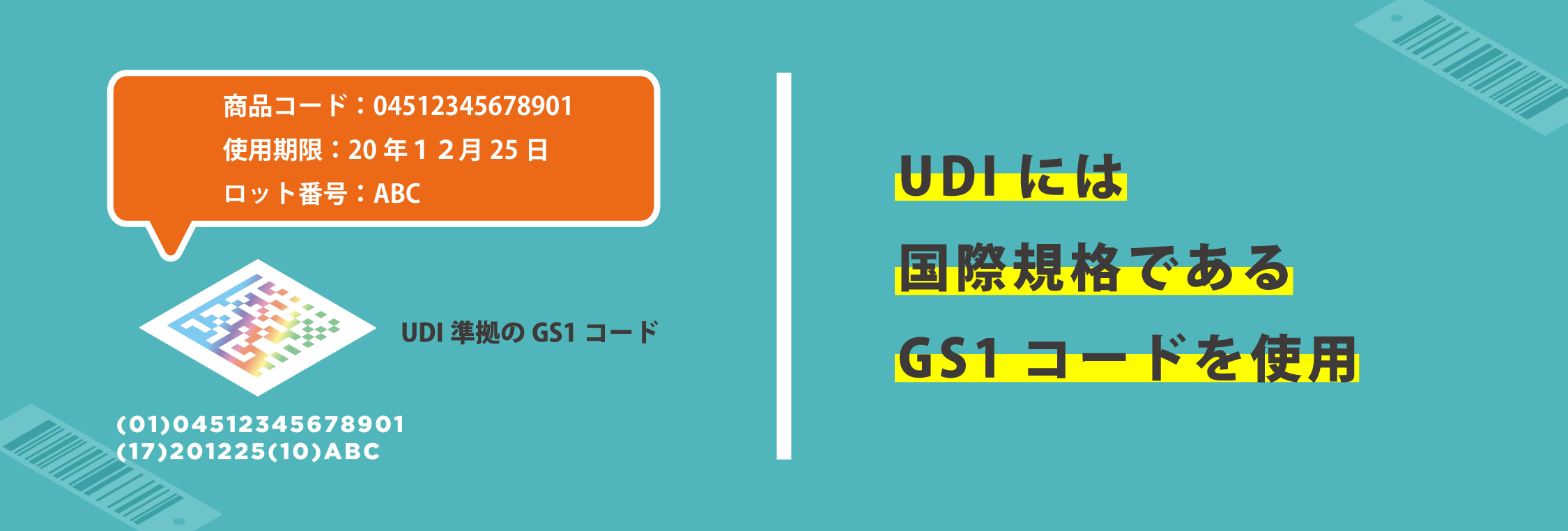
UDIを用いた国際的な医療機器データベース|GUDID
GUDIDとは?
GUDID(Global UDI Database)とは、UDIを使用した医療機器国際的なデータベースです。登録された医療機器等の詳細データを確認することができます。

GUDIDのデータベースはU.S.NATIONAL LIBRARY OF MEDICHINEの以下のURLより確認できます。
https://accessgudid.nlm.nih.gov/
アメリカではUDI準拠のGS1コードの表記だけでなく、2014年9月から*段階的にGUDIDへの登録が義務化され、2020年9月を目処にほぼ全ての医療機器の登録が必要となります。欧州においても2017年5月に医療機器規則が公布され、2020年5月から米国と同様のUDI 規制が開始される予定です。
*生命維持装置などの個体管理の優先度の高い製品(高度管理医療機器クラス3)

日本国内は法令ではない?|日本国内でのUDIの活用
日本国内ではUDI活用は厚生労働省の行政通知に留まり、法令ではありません。厚生労働省および医療機器・薬品業界の主導で、1999年からGS1コードを活用した医療機器へのバーコード表示と日本独自の医療機器データベースへの登録が進みました。欧米諸国に先立ち、医療機器や医薬品の個装箱に関しては現在でも欧米に比べより多くの商品にすでにGS1コードが表示されています。その一方で、医療機器本体へのUDIコード(GS1)の表示は対象外であることや欧米諸国で採用されるUDIとは表記の差異があることや、医療機関内部での運用が拡がらないといった課題があります。
また日本国内では1次元コードのGS1-128が原則として使用されていますが、海外では印字スペースが狭く、汚れなどのダメージにも強い2次元コードのGS1-Datamatrixが使用されるケースが多いです。

1次元バーコードリーダーではGS1-Datamatrixの読み取りができないため、輸入した医療機器についた2次元コードリーダーを新たに導入する必要があります。
海外輸出時にはUDI対応が必要
GS1コードの印字規格
UDIに使用されるGS1コードには国際的な印字規格が存在します。特に海外で使用されるGS1 -DatamatrixはISO/IEC 16022(JIS X0512)で規定されているデータマトリックスをベースに、GS1 アプリケーション識別子を使用できるようにしたもので、コードの印字サイズなどの規定が印刷される対象や読み取られる環境によって細かく定められています。

UDI 規則への対応のために欧米諸国への医療機器輸出時には必ず製品へのGS1コードの表示が必要であり、国内では使用が進んでいないGS1-Datamatrixには規格に準拠した印字を遵守する必要があります。輸出先の規制や業界ルールに沿わないGS1コードを印字してしまうことでバーコードリーダーで読み取れないといった納入時のトラブルやGUDIDでの照合ができず法令違反となってしまうといったトラブルなどを避けるため、国際規格であるGS1コードへの正しい理解と各国の規制・業界ルールの把握が重要です。

GS1コード検証の標準機
GS1から認定を受けたLVSシリーズのバーコード検証機は、GS1総合仕様書(GS1 General Specification)などの国際的な印字規格の検証が可能です。医療機器メーカー様や医薬品製造メーカー様に数多くご採用いただいております。導入前のご評価用にお貸出しデモ機をご用意しております。LVSシリーズ・バーコード検証機の製品詳細はページ下部の関連製品をご参照ください。












